1.1.Sistema Periódico De Mendeleive.
Mendeleiev se basó principalmente en las propiedades químicas (tipos de óxidos, tipos de hidruros, valencia, etc..). Según Mendeleiev – las propiedades de los elementos era una función periódica de su peso atómico- lo que llamó “Ley periódica de los elementos”.
Descripción de la tabla de Mendeleiev:
1. Los 63 elementos conocidos hasta ese entonces fueron ordenados en funcion creciente a su peso atómico en filas horizontales y grupos (columnas)
2. Los elementos de un mismo grupo poseen propiedades semejantes, por ejemplo forman óxidos e hidruros de fórmula idéntica. Los elementos de cada fila forman un “Periodo”, que indica el número de niveles de energía.
3. Los elementos de cada columna, que forman un “Grupo”, poseen propiedades semejantes y se subdividen en familias A y B; los grupos generalmente indican los electrones del último novel de energía. En este ordenamiento los elementos con propiedades similares están en un mismo grupo.
4. Mendeleiev observó que para ordenar en grupos, era necesario dejar espacios o casilleros vacíos para nuevos elementos aún no descubiertos o incluso le puso nombre a cada uno de estos elementos no conocidos utilizando: eka = primero y dvi = segundo.
Ley periódica de Mendeleiev:
Mendeleiev observó que las propiedades de los elementos se repetían periódicamente; es por ello que la tabla periódica se conoce como “tabla periódica de los elementos” y enunció la siguiente Ley Periódica:
“Las propiedades de los elementos son función periódica a sus masas atómicas
Ventajas de la tabla de Mendeleiev:
1. Permitió determinar nuevas propiedades de los elementos.
2. Permitió tener una idea mas general de la clasificación de los elementos.
3. Predijo la existencia de nuevos elementos , por ejemplo: Escandio, Germanio y Renio.
4. En su época Mendeleiev clasificó a 63 elementos que conocía y para predecir las propiedades de los elementos no descubiertos, determinó que las propiedades de los elementos se encontraban relacionadas con los elementos que los circundaban.
5. En 1984, Ramsay descubrió un gas al que denominó Argón. Es monoatómico, no presenta reacciones químicas y carecía de un lugar en la tabla. Inmediatamente supuso que debian existir otros gases de propiedades similares y que todos juntos formarian un grupo. En efecto, pocod espués se descubrierón los otros gases nobles y se les asignó el grupo cero.
6. Todos los espacios que dejó en blanco se fueron llenando al descubrirse los elementos correspondientes. Estos presentaban propiedades similares a las asignadas por Mendeleiev.
El químico ruso Dimitri Mendeleiev y el alemán Lothar Meyer, en base a trabajos de investigación que realizaron simultánemente e independientemente publicaron una “tabla periódica de los elementos”, siendo la primera tabla periódica que se realizó.
1.2. Triadas De Dobereiner 1829
A principios del siglo XIX, se conocían la suficiente cantidad de elementos y compuestos como para que fuese necesario hacer una clasificación con el fin de facilitar su comprensión y estudio.
Desde el principio se supo de la existencia de familias de elementos que compartían propiedades y semejanzas entre sí, intuyéndose que debía de existir una ley natural que tendiese a agrupar y relacionar con lógica a los elementos. La búsqueda de esta ley está llena de intentos, como las Triadas de Döbereiner , las octavas de Newlands, el tornillo telúrico de Charcourtois, etc, todos ellos basados generalmente en dos criterios fundamentales:
Desde el principio se supo de la existencia de familias de elementos que compartían propiedades y semejanzas entre sí, intuyéndose que debía de existir una ley natural que tendiese a agrupar y relacionar con lógica a los elementos. La búsqueda de esta ley está llena de intentos, como las Triadas de Döbereiner , las octavas de Newlands, el tornillo telúrico de Charcourtois, etc, todos ellos basados generalmente en dos criterios fundamentales:
- La similitud de las propiedades fisicoquímicas de los elementos
- La relación entre las propiedades y alguna característica atómica como la masa atómica.
Muchos de los intentos por encontrar una forma de agrupación o clasificación de los elementos, ya sea por su originalidad o por su éxito merecen un reconocimiento, y este es el caso de las Triadas de Döbereiner.
Las Triadas de Döbereiner, fue uno de los primeros intentos de clasificación de los elementos químicos, según la similitud de las propiedades, relacionando sus pesos atómicos. Esta clasificación fue realizada por Johann Wolfgang Döbereiner, un químico alemán, que entre otras cosas también estudió los fenómenos de catálisis.
Döbereiner, en 1817, declaró la similitud entre las propiedades de algunos grupos de elementos, que variaban progresivamente desde el primero al último. Veinte años después, en 1827, destacó la existencia de otras agrupaciones de tres elementos, que seguían una análoga relación entre sí.
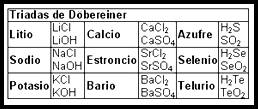
Estos grupos eran:
- Cloro, bromo y yodo
- Azufre, selenio y telurio
- Litio, sodio y potasio
A estos grupos de elementos, agrupados de tres en tres, se le conoció con el nombre de triadas.
De estos grupos de tres se continuaron encontrando, hasta que en 1850 ya se tenía conocimiento de entorno a 20 triadas.
De estos grupos de tres se continuaron encontrando, hasta que en 1850 ya se tenía conocimiento de entorno a 20 triadas.
Döbereiner hizo un intento de relacionar las propiedades y semejanzas químicas de los elementos y de sus compuestos, con las características atómicas de cada uno de ellos, que en ese caso se trataba de los pesos atómicos, viéndose un gran parecido entre ellos, y una variación progresiva y gradual desde el primero hasta el tercero o último de la triada.
En la clasificación de las triadas (ordenamiento de tres elementos), el químico alemán intentó explicar que el peso atómico medio de los elementos que se encuentran en los extremos de las triadas, es similar al peso atómico de los elementos que se encuentran en la mitad de la triada. Por ejemplo: la triada Cloro, bromo y Yodo, tiene respectivamente 36,80, y 127 respectivamente, en cuanto al peso atómico se refiere. Si realizamos la suma de los extremos, es decir 36+127 y a su vez, la dividimos entre 2, el resultado es 81, o lo que es lo mismo, un número próximo a 80, que casualmente es el número atómico del elemento del medio, es decir, del bromo, hecho que hace que encaje perfectamente en el ordenamiento de la triada.
Triadas de Döbereiner | La Guía de Química http://quimica.laguia2000.com/general/triadas-de-dobereiner#ixzz4Lh4UkemR
1.3.Anillo De Chancourtois 1862.
Alexander Emile Beguyer de Chancourtois, geólogo y profesor de l'Ecole de Mines de Paris estudió la clasificación y sistematización en Mineralogia. Necesitaba un sistema de sustancies simples para estudios litológicos y por eso comenzó a trabajar en una clasificación basada en los principios entonces en uso: clase, orden, etc.
En 1862 envió a la Academie de Sciences de Paris un informe donde proponía una clasificación de los elementos químicos colocados sobre la superfície de un cilindro. Los elementos se disponían sobre una linia diagonal formando un angulo de 45 º con la horizontal, dibujando una espiral y estaban ordenados según su peso atómico creciente (expresados en números enteros), de manera que los que tenían propiedades parecidas se situaban en una misma línia vertical. Chancourtois fue el primero en darse cuenta de que las propiedades de los elementos eran una función de su peso atómico. El sistema era más complejo pues también incluía compuestos (óxidos, amoníaco,) y aleaciones. Además el esquema resultaba complicado técnicamente de imprimir por lo que en su comunicación no se incluyó. Probablemente este hecho influyó en que su propuesta no fue demasiado conocida.
. Alexandre construyó una hélice de papel en la que los elementos estaban ordenados por pesos atómicos, arrollada sobre un cilindro vertical, posteriormente con el químico ingles Newlands proponen la Ley de las octavas que enuncia que las propiedades se repiten cada ocho elementos; por ello no se pudieron aplicar a elementos más allá del calcio por lo cual la clasificación de esta tabla es todavía insuficiente.
Hay que recalcar que esta tabla periódica fue inconsistente debido a que no funcionó para todos los elementos, pero sirvió como punto de apoyo para Mendeleev que siguió con la investigación y construcción de un nuevo modelo de tabla periódica, además todo este conjunto de investigaciones nos llevan a la que hoy en día es llamada Tabla periódica actualizada de los elementos químicos.
Hay que recalcar que esta tabla periódica fue inconsistente debido a que no funcionó para todos los elementos, pero sirvió como punto de apoyo para Mendeleev que siguió con la investigación y construcción de un nuevo modelo de tabla periódica, además todo este conjunto de investigaciones nos llevan a la que hoy en día es llamada Tabla periódica actualizada de los elementos químicos.
Chancourtois fue un químico francés quien ordenó los elementos químicos en función creciente a su peso atómico sobre una curva helicoidal que envolvía a un cilindro, cuya base circular fue dividida en 16 partes iguales. Esta curva helicoidal tenia la particularidad de que si por una parte trazábamos una linea vertical, intersectaba a los elementos con propiedades.

1.4.Octavas De Newlands 1864.
El químico inglés Jhon Alexander Reina Newlands, propuso el ordenamiento de los elementos, según el orden creciente de sus masas atómicas, dando un gran paso en la correcta clasificación de los elementos.
Newlands dispuso a los elementos en filas horizontales de 7 en 7, resultando periodos en que el octavo elemento se parecía en propiedades al primero; el noveno al segundo; el décimo al tercero y así sucesivamente. Por lo cual los que tengas propiedades semejantes tienen que quedar en la misma columna.

En 1865, el químico inglés John Alexander Reina Newlands, intentó solucionar el problema del comportamiento periódico de los elementos, colocando los elementos más ligeros en orden creciente según sus pesos atómicos de la siguiente manera:
| Li | Be | B | C | N | O | F |
| Na | Mg | Al | Si | P | S | Cl |
| K | Ca |
Newlands se dio cuenta que el octavo elemento se asemejaba al primero, así como el noveno era similar al segundo, etc. A esta observación se le llama, “Ley de las octavas de Newland”, en honor al químico inglés.
Como cada ocho elementos, aparecía otro elemento de iguales propiedades, a Newlands se le ocurrió hacer la comparación entre sus octavas, con las octavas musicales, observando que la periodicidad de las octavas químicas, sugería una armonía como si de música se tratase. Dicha comparación, a pesar de ser idílica y atractiva, carecía de validez alguna, pero fue por ella que a su clasificación le dio el nombre de
osteriormente se descubrió una familia de compuestos inertes, formada por el helio, neón, argón, kriptón, y xenón, o lo que es lo mismo, el grupo de los gases nobles. Este descubrimiento transformó a las octavas de Newlands, en novanas.
Los esfuerzos de Newlands, supusieron un gran paso con buena dirección, en los que a clasificación de elementos se refería pero, sin embargo, pueden destacarse tres grandes críticas a su esquema clasificatorio:
- No existía un lugar indicado para los elementos recientemente descubiertos.
- No tuvo mucha consideración con los pesos atómicos, ni siquiera realizó una estimación aproximativa de los valores más probables.
- Algunos elementos no encajaban en el esquema de Newlands , como por ejemplo , el cromo, que quedaba mal posicionado bajo el aluminio, y el magnesio, que es un metal, venía colocado bajo el fósforo que es un no metal, así como el hierro que tratándose de un metal, se encontraba debajo del azufre (no metálico), así que tanto éstos, como otros elementos, no encajaban de ninguna manera en el esquema.
Esta clasificación, o regla de ordenación, a partir del calcio en adelante, no se cumplía, por lo que no fue destacada por la comunidad científica, la cual incluso se burló de dicha clasificación, pero 23 años después, fue finalmente reconocida por la Royal Society, otorgando a Newland la medalla Davy, que era la más alta condecoración dada por esta sociedad.
Las tres primeras filas de la tabla de Newlands, en cuanto a puntos de ebullición y fusión, se puede comparar a la tabla periódica actual.
: Ley de las octavas de Newlands | La Guía de Química http://quimica.laguia2000.com/general/ley-de-las-octavas-de-newlands#ixzz4Lh8FrFHb

No hay comentarios:
Publicar un comentario